云浮浩林企業(yè)管理咨詢被吊銷營(yíng)業(yè)執(zhí)照的警示與啟示
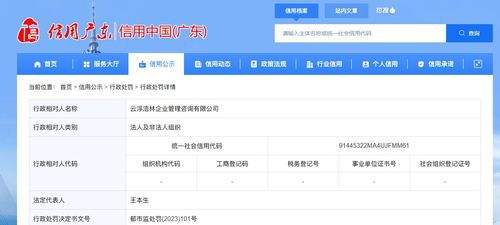
近日,云浮浩林企業(yè)管理咨詢有限公司因違規(guī)經(jīng)營(yíng)被吊銷營(yíng)業(yè)執(zhí)照,這一事件引發(fā)了業(yè)界對(duì)企業(yè)管理咨詢行業(yè)規(guī)范性的關(guān)注。企業(yè)管理咨詢作為幫助企業(yè)提升運(yùn)營(yíng)效率、優(yōu)化組織結(jié)構(gòu)的重要服務(wù)領(lǐng)域,其合規(guī)經(jīng)營(yíng)不僅關(guān)系到企業(yè)自身的生存,更直接影響客戶企業(yè)的信任與發(fā)展。此次浩林公司被吊銷執(zhí)照,據(jù)相關(guān)通報(bào)顯示,主要原因可能涉及虛假宣傳、未履行合同義務(wù)或違反行業(yè)管理規(guī)定等行為。這起事件警示所有從事管理咨詢的企業(yè):必須嚴(yán)格遵守法律法規(guī),堅(jiān)持誠(chéng)信經(jīng)營(yíng),避免急功近利。同時(shí),也提醒企業(yè)在選擇咨詢服務(wù)時(shí),應(yīng)審慎核查對(duì)方資質(zhì),優(yōu)先考慮有良好口碑和正規(guī)許可的機(jī)構(gòu)。行業(yè)監(jiān)管需進(jìn)一步加強(qiáng),通過(guò)完善標(biāo)準(zhǔn)和強(qiáng)化執(zhí)法,推動(dòng)企業(yè)管理咨詢市場(chǎng)向?qū)I(yè)化、透明化方向發(fā)展,為實(shí)體經(jīng)濟(jì)注入更多正能量。
如若轉(zhuǎn)載,請(qǐng)注明出處:http://m.gsxxcx.cn/product/14.html
更新時(shí)間:2026-03-15 19:46:22